Maddenin Halleri
Maddenin Halleri: Giriş
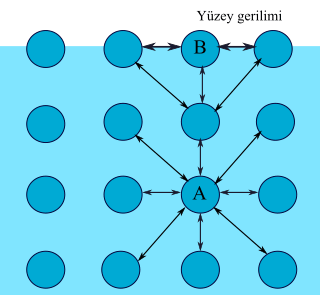
Uzayda yer kaplayan her şeye madde denir. Maddeler kütleye ve hacme sahiptir. Maddeler belirli basınç ve sıcaklıklarda maddenin 4 temel halinden birisinde bulunabilir; katı, sıvı, gaz ve plazma. Maddeleri oluşturan moleküllerin davranışları maddenin her halinde değişiktir.
Maddenin 3 Hali: Katı – Sıvı – Gaz
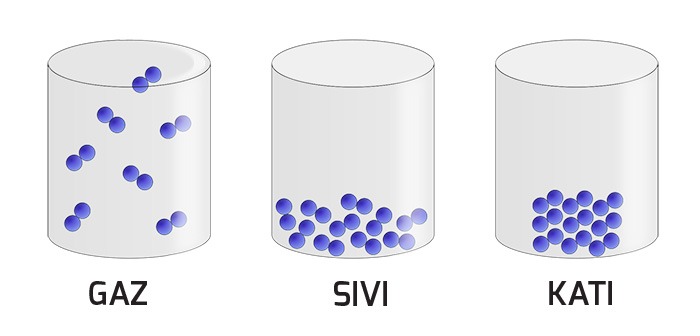
Maddenin katı, sıvı ve gaz hallerini kıyaslamamız gerekirse; genellikle katı maddeler maddenin en düzenli ve moleküllerin birbirine belirli bir düzende sıkı bir şekilde bağlandığını gözlemleriz. Moleküller arası bağlar sıvılarda şiddetini azaltır ve bu yüzden sıvıların belirli bir şekli bulunmaz. Gazlarda ise bu bağlar yok denecek kadar güçsüzleşir.
Kısacası, moleküller arası bağların kuvveti maddenin katı, sıvı veya gaz halde bulunmasını etkiler. Bir maddenin molekülleri arasındaki bağ ne kadar güçlüyse, kaynama ve erime sıcaklıkları da o kadar yüksek olur.
Suyun Özel Durumu
Hal Değişimi
Hal değişimi, maddenin fiziksel özelliğinin değiştiği ancak kimyasal özelliğinin sabit kaldığı bir tür değişimdir. Bu değişim, moleküller arasındaki etkileşimlerin (zayıf etkileşimlerin) değişmesinden kaynaklanır.
Örneğin, su katıdan sıvıya geçerken hidrojen bağlarının kuvveti zayıflar. Bu durumun tersine, su sıvıdan katıya geçerken hidrojen bağlarının kuvveti artar. Taneciklerin yapısında kimyasal bir değişim olmaması nedeniyle, hal değişimleri fiziksel değişimlere örnektir.
Hal değişimleri şu şekilde sınıflandırılabilir:
- Erime (Sıvı Haline Geçme): Katının sıcaklığı arttıkça moleküler düzeni bozularak sıvı hale geçer. Bu duruma erime denir. Erime noktası, katının sıvı hale geçtiği belirli bir sıcaklığı ifade eder.
- Donma (Katılaşma): Sıvının soğutulmasıyla moleküler düzen artar ve sıvı katı hale geçer. Bu olaya donma denir. Donma noktası, sıvının katı hale geçtiği belirli bir sıcaklığı ifade eder.
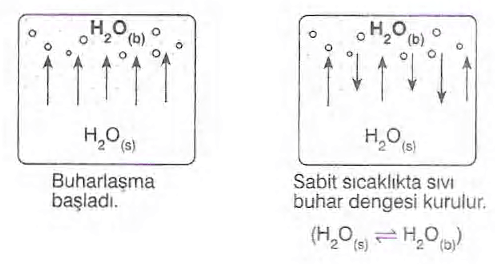
- Buharlaşma: Sıvının ısı alarak gaz hale geçme sürecidir. Buharlaşma genellikle sıcaklık arttıkça hızlanır.
- Yoğuşma: Gazın soğutularak sıvı hale geçmesidir. Yoğuşma genellikle sıcaklık azaldıkça gerçekleşir.
- Süblimleşme: Katının doğrudan gaz hale geçmesi olayına süblimleşme denir. Süblimleşme, katının buharlaşma noktasının altında bir sıcaklıkta oluşabilir.
Hal değişimleri, maddeyi oluşturan taneciklerin arasındaki etkileşimlerin enerji alışverişiyle gerçekleşir ve bu değişimler sıcaklık ve basınç gibi faktörlere bağlı olarak meydana gelir.
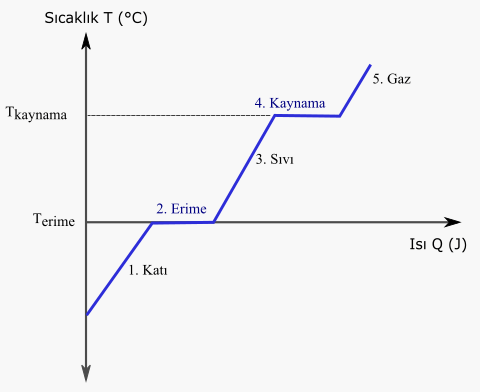
Katı – Sıvı Hal Değişimleri
Katı halde tanecikler sıkı bir yapıda bulunurken, sıvı veya gaz hallerinde moleküller arasındaki etkileşim daha gevşektir. Bu nedenle, katıların sıvı veya gaz haline geçebilmesi için ısı alması gereklidir.
Erime
Katının ısı alarak sıvı hale geçme sürecine erime denir. Erime olayının gerçekleştiği sıcaklığa erime noktası adı verilir. Saf bir maddenin sıvısının donma noktası ile katısının erime noktası genellikle aynıdır. Erime sırasında katı, ısı alarak sıvıya dönüşür ve bu süreç boyunca sıcaklık değişmez.
Donma
Sıvının ısı vererek katı hale dönmesine donma denir. Donma noktası, donma olayının gerçekleştiği sıcaklığı ifade eder. Saf bir maddenin sıvısının donma noktası ile katısının erime noktası genellikle aynıdır. Donma sırasında sıvı, ısı vererek katıya dönüşür ve bu süreç boyunca sıcaklık değişmez.
Sıvı – Gaz Hal Değişimleri
Sıvı molekülleri arasındaki etkileşim, katılardan daha zayıf olup gazlardan daha kuvvetlidir. Bu nedenle, sıvılar ısı alarak gaz, ısı vererek ise katı hale dönüşebilir.
Buharlaşma
Sıvıların ısı alarak gaz haline geçmesine buharlaşma denir. Buharlaşma, her sıcaklıkta gerçekleşebilir ve örneğin, 20 derecede asılan çamaşırların kuruması veya 40 derecede asılan çamaşırların kuruması gibi farklı sıcaklıklarda meydana gelebilir.
Yoğuşma
Gazın ısı vererek sıvı hale geçmesine yoğuşma denir. Yoğuşma, buharlaşmanın tam tersidir ve genellikle su döngüsü gibi doğal olaylarda görülür.
Katı – Gaz Hal Değişimleri
Süblimleşme
Bazı katılar, ısı aldıklarında sıvı hale geçmeden doğrudan gaz haline geçer. Bu olaya süblimleşme denir.
Kırağılaşma
Gaz haldeki bir madde, ısı vererek doğrudan katı hale geçtiğinde bu olaya kırağılaşma denir.
Katı Türleri
Maddeler, katı, sıvı, gaz ve plazma olmak üzere dört farklı halden birinde bulunabilirler. Maddeler arasında en düzenli yapıya sahip olanlar katılardır. Katı maddelerin kimyasal yapıları (atom, iyon veya moleküller) düzenli bir şekilde yerleşmiştir.
Tüm maddeler, yeteri kadar soğutulduğunda katı hale geçer. Oluşan katıların özellikleri, katıyı oluşturan atom, iyon veya molekülleri bir arada tutan kuvvetlere bağlıdır.
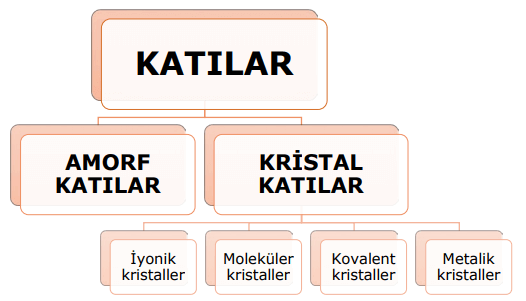
Katıların yapısını incelediğimizde, görünüş ve özellik açısından farklı katı türlerinin bulunduğunu gözlemleriz. Bazı katılar serttir ve elektriği iyi iletir, bazıları ise yumuşak ve istenilen şekli alabilen katılardır; hatta bazıları elektriği iletemez. Katılar genellikle amor katılar ve kristal katılar olarak iki ana başlık altında incelenebilir.
Amorf Katılar
Amorf katıları oluşturan tanecikler, gelişi güzel ve düzensiz bir şekilde istiflenmiştir. Bu nedenle, amorf katıların belirli bir şekli yoktur. Cam, lastik, mumlar ve tereyağı gibi maddeler amorf katılara örnek olarak verilebilir. Bu katıların belirli bir erime veya donma noktası yoktur. Isıtıldıklarında belirli bir sıcaklıkta yumuşar ve akışkanlık kazanırlar. Bu yumuşama noktasına “camsı geçiş sıcaklığı” denir.
Kristal Katılar
Kristal katıları oluşturan tanecikler ise düzenli bir şekilde istiflenmiştir. Bu nedenle, kristal katıların belirli bir şekli vardır. Kristal katılar, iyonik, moleküler, kovalent ve metalik kristaller olmak üzere farklı sınıflara ayrılır. İyonik kristaller, iyonlardan oluşur ve iyonik bağlarla birbirlerine bağlıdır. Moleküler kristallerde moleküller arasındaki çekim kuvveti zayıftır. Kovalent kristallerde tanecikler arasında her doğrultuda kovalent bağlar bulunur. Metalik kristaller ise metallerin değerlik elektronlarının serbestçe hareket ettiği bir yapıya sahiptir ve metalik bağlarla birbirine bağlıdır.
- Amorf Katılar:
Amorf katıları oluşturan tanecikler rastgele ve düzensiz bir şekilde yerleştirilmiştir. Bu nedenle, amorf katıların belirli bir şekli yoktur ve dış müdahale olmadan doğal bir biçimleri oluşmaz. Cam, lastik, mumlar, ve tereyağı gibi maddeler bu kategoriye örnek olarak verilebilir. Amorf katıların belirli bir erime veya donma noktası yoktur. Isıtıldıklarında belirli bir sıcaklıkta yumuşarlar ve akışkanlık kazanırlar, bu şekilde şekillendirilebilirler. Amorf katının yumuşamaya başladığı sıcaklığa “camsı geçiş sıcaklığı” denir. - Kristal Katılar:
Kristal katıları oluşturan tanecikler düzenli bir şekilde yerleştirilmiştir. Bu düzen, kristal katılara belirli bir şekil ve yapı kazandırır. Kristal katıların belirli bir erime ve donma noktası vardır. Yüzeyleri genellikle düzdür ve geometrik şekillerden oluşur. Altın, sodyum klorür ve elmas gibi maddeler kristal yapılı katılara örnektir. Kristal katılar iyonik, moleküler, kovalent ve metalik kristaller olmak üzere dört farklı sınıfa ayrılır.a) İyonik Kristaller:
İyonik kristalleri oluşturan tanecikler iyonlardır ve aralarında iyonik bağlar bulunur. Bu bağlar kuvvetli olduğundan, iyonik kristallerin erime noktaları yüksektir. Ancak, katı haldeki iyonlar serbestçe hareket edemedikleri için elektrik akımını iletemezler.b) Moleküler Kristaller:
Şeker veya buz gibi maddeler moleküler kristallere örnektir. Moleküler kristallerde, moleküller arasındaki çekim kuvveti iyonik ve kovalent bağlara oranla daha zayıftır, bu nedenle erime ve kaynama noktaları düşüktür.c) Kovalent Kristaller:
Kovalent kristallerde tanecikler arasında her yönde kovalent bağlar bulunur. Bu kristallerin erime noktaları çok yüksektir ve oldukça sertlerdir.d) Metalik Kristaller:
Metalik kristallerde, metallerin değerlik elektronları komşu metal atomlarının boş değerlik orbitallerine geçebilir. Oluşan elektron denizi içinde (+) yüklü metal iyonları meydana gelir. Metalik kristaller değerlik elektron sayısına bağlı olarak farklı erime ve kaynama noktalarına sahiptir, elektrik akımını iyi iletirler ve parlak bir yüzeye sahiptirler.